
Предельные углеводороды

Алканы (предельные, насыщенные, парафины) – органические вещества, состоящие из атомов углерода и водорода, связанных между собой одинарными (сигма) связями.
Строение
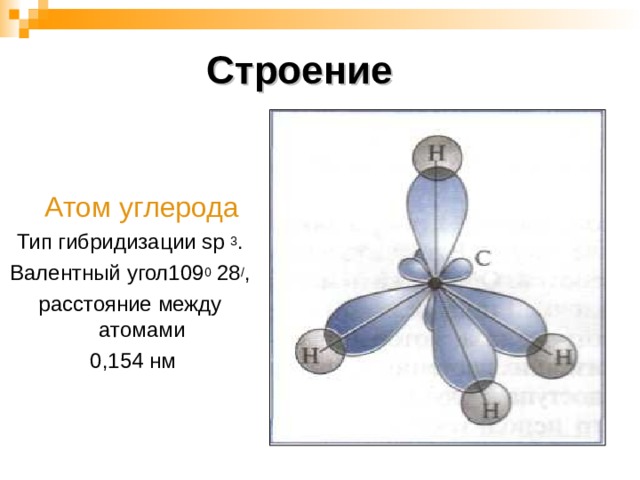
Атом углерода
Тип гибридизации sp 3 .
Валентный угол109 0 28 / ,
расстояние между атомами
0,154 нм
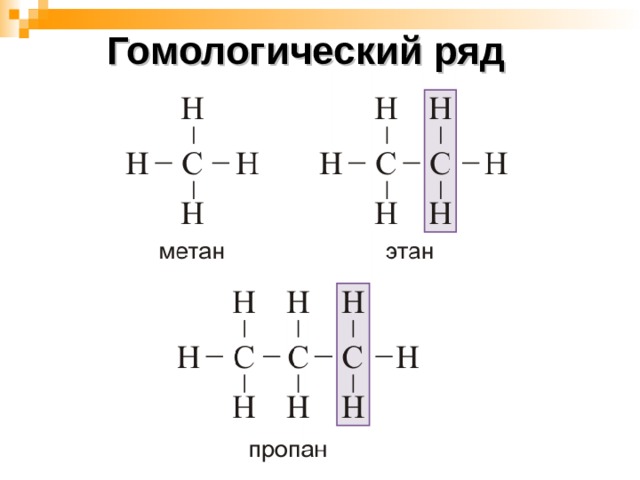
Гомологический ряд
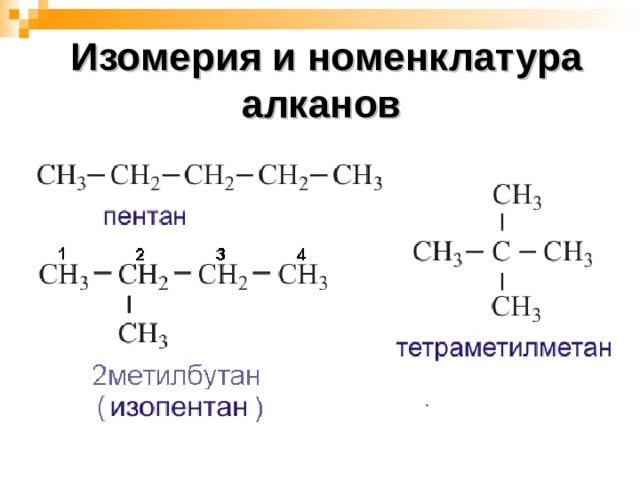
Изомерия и номенклатура алканов

Нахождение в природе:
- Природный газ на 75%-85% состоит из метана, от 25%-2% этана, пропана и других соединений.
- Нефть и ископаемый уголь (содержат не чистые углеводороды)
- Месторождения угля (бурого), нефти, газа на Дальнем Востоке: шельфовая зона о.Сахалин, Райчихинское месторождение (Амурская обл.), п.Чегдомын,г. Дальнегорск

Физические свойства
- С 1 – С 4 – газ без цвета и запаха
- С 5 – С 17 – бесцветные жидкости с запахом бензина
- С 18 … - твердые вещества, белого цвета, жирные на ощупь
- По мере увеличения числа атомов углерода в цепи возрастает температура кипения, плавления и плотность
- Молекулы с разветвленным скелетом кипят и плавятся при более низкой температуре, чем молекулы с нормальным строением
- Газообразные и жидкие алканы образуют взрывоопасные смеси с воздухом
- Алканы практически не растворимы в воде, но растворяются в неполярных органических растворителях (бензол,тетрахлорметан)
- Жидкие и твердые алканы смешиваются друг с другом
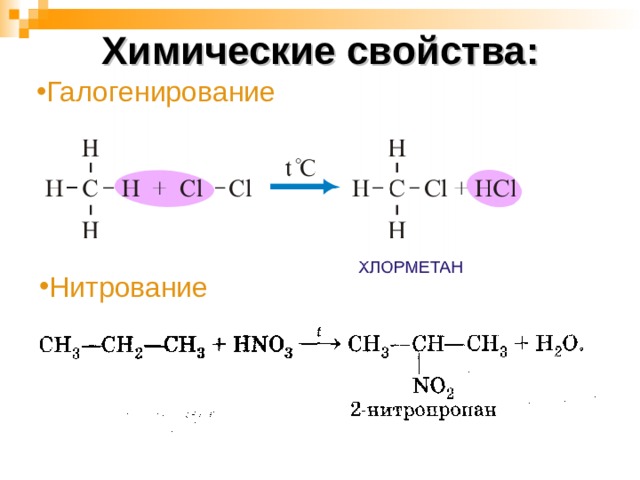
Химические свойства:
- Галогенирование
- Нитрование
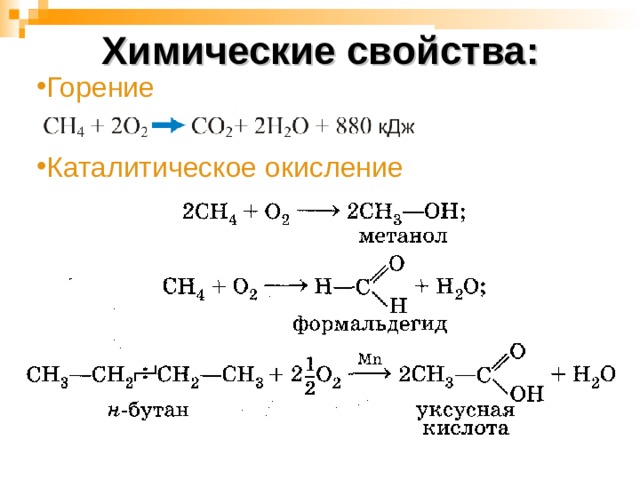
Химические свойства:
- Горение
- Каталитическое окисление

Химические свойства:
- Пиролиз ( t выше 600 градусов С)
- Крекинг ( t ниже 600 градусов С)
- Изомеризация
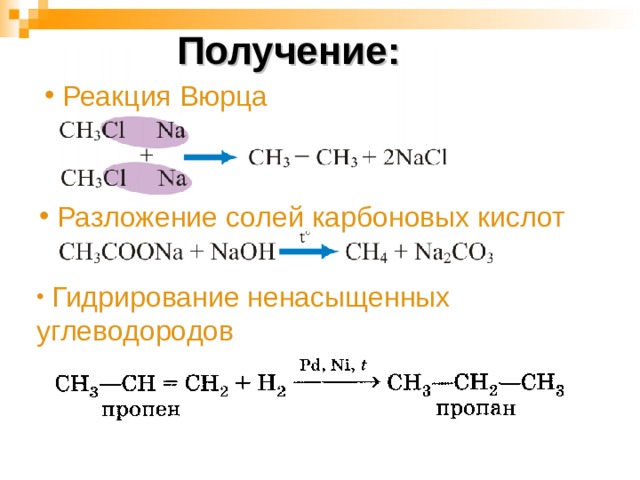
Получение:
- Реакция Вюрца
- Разложение солей карбоновых кислот
- Гидрирование ненасыщенных углеводородов
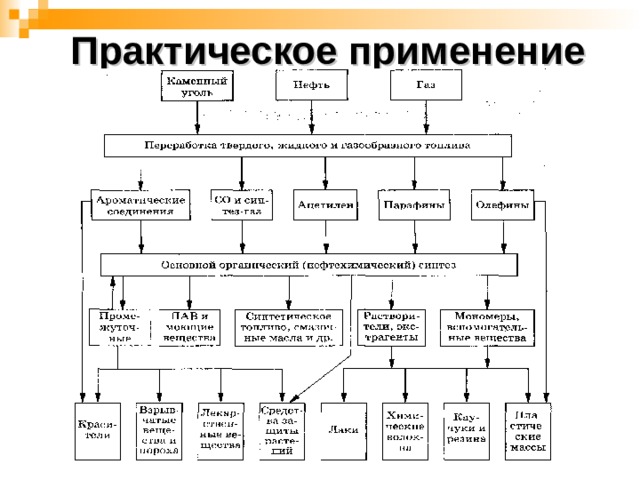
Практическое применение





