Кислоты. Cпособы получения и химические свойства
Кислоты – сложные вещества, которые при взаимодействии с водой образуют в качестве катионов только ионы Н+ (или Н3О+).
По растворимости в воде кислоты можно поделить на растворимые и нерастворимые. Некоторые кислоты самопроизвольно разлагаются и в водном растворе практически не существуют (неустойчивые).

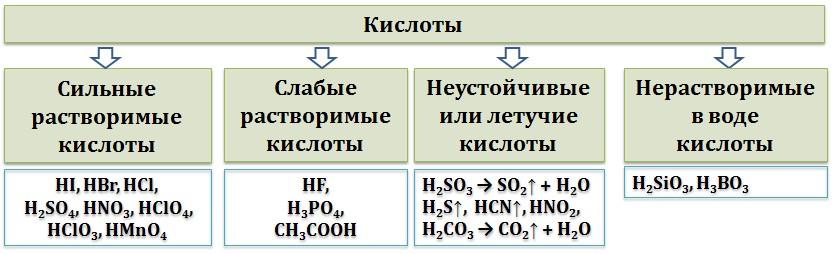 Получение кислот
Получение кислот
1. Взаимодействие кислотных оксидов с водой. При этом с водой реагируют при обычных условиях только те оксиды, которым соответствует кислородсодержащая растворимая кислота.
кислотный оксид + вода = кислота
Например, оксид серы (VI) реагирует с водой с образованием серной кислоты:
SO3 + H2O → H2SO4
При этом оксид кремния (IV) с водой не реагирует:
SiO2 + H2O ≠
Поэтому можно получить из солей кремневой кислоты
Na2 SiO3 + 2HCl = 2NaCl + H2SiO3↓
2. Взаимодействие неметаллов с водородом. Таким образом получают только бескислородные кислоты.
Неметалл + водород = бескислородная кислота
Например, хлор реагирует с водородом:
H20 + Cl20 → 2H+Cl—
3. Электролиз растворов солей. Как правило, для получения кислот электролизу подвергают растворы солей, образованных кислотным остатком кислородсодержащих кислот.
Например, электролиз раствора сульфата меди (II):
2CuSO4 + 2H2O → 2Cu + 2H2SO4 + O2
4. Кислоты образуются при взаимодействии других кислот с солями. При этом более сильная кислота вытесняет менее сильную.
Например: карбонат кальция CaCO3 (нерастворимая соль угольной кислоты) может реагировать с более сильной серной кислотой. При этом образуется боле слабая угольная кислота.
CaCO3 + H2SO4 → CaSO4 + 2H2O + CO2
Соль слабой кремниевой кислоты + сильная соляная кислота , получается слабая кремниевая кислота
Na2 SiO3 + 2HCl = 2NaCl + H2SiO3↓
5. Кислоты можно получить окислением оксидов, других кислот и неметаллов в водном растворе кислородом или другими окислителями. 4N+4O2 + 2H2O + O2 = 4HN+5O3
Например, концентрированная азотная кислота окисляет фосфор, S, C, I2 до cоответствующих кислот:
P + 5HNO3 → H3PO4 + 5NO2 + H2O
S + 6HNO3 = H2SO4 + 6NO2 + 2H2O
I2 + 10HNO3(конц.) (t)→ 2HIO3 + 10NO2↑ + 4H2O
C + 4HNO3(конц.) → CO2↑ + 2H2O + 4NO2↑
Химические свойства кислот1. В водных растворах кислоты диссоциируют на катионы водорода Н+ и анионы кислотных остатков. При этом сильные кислоты диссоциируют почти полностью, а слабые кислоты диссоциируют частично.
Например, соляная кислота диссоциирует почти полностью:
HCl → H+ + Cl–
Если говорить точнее, происходит протолиз воды, и в растворе образуются ионы гидроксония:
HCl + H2O → H3O+ + Cl–
Многоосновные кислоты диссоциируют cтупенчато.
Например, сернистая кислота диссоциирует в две ступени:
H2SO3 ↔ H+ + HSO3–
HSO3– ↔ H+ + SO32–
Фосфорная кислота диссоциирует в 3 ступени:
Н3PO4 ↔ H+ + H2PO4–
H2PO4–↔ H+ + HPO42–
HPO42– H+ + PO43–
2. Кислоты изменяют окраску индикатора. Водный раствор кислот окрашивает лакмус в красный цвет,
метилоранж в красный цвет. Фенолфталеин не изменяет окраску в присутствии кислот.
3. Кислоты взаимодействуют с металлами.
При этом протекает окислительно-восстановительная реакция. Однако минеральные кислоты и кислоты-окислители взаимодействуют по-разному.
К минеральным кислотам относятся соляная кислота HCl, разбавленная серная кислота H2SO4, фосфорная кислота H3PO4, плавиковая кислота HF, бромоводородная HBr и йодоводородная кислоты HI.
Такие кислоты взаимодействуют только с металлами, расположенными в ряду активности до водорода:
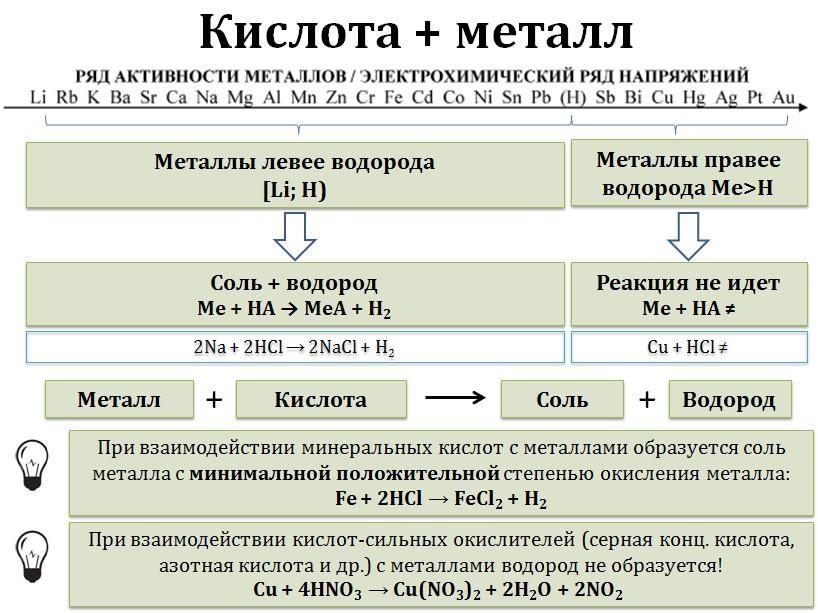
При взаимодействии минеральных кислот с металлами образуются соль и водород:
минеральная кислота + металл = соль + H2↑
Например, железо взаимодействует с соляной кислотой с образованием хлорида железа (II):
Fe + 2H+Cl → Fe+2Cl2 + H20
Cu + H+Cl ≠
Сероводородная кислота H2S, угольная H2CO3, сернистая H2SO3 и кремниевая H2SiO3 с металлами не взаимодействуют.
Кислоты-окислители (азотная кислота HNO3 любой концентрации и серная концентрированная кислота H2SO4(конц)) при взаимодействии с металлами водород не образуют, т.к. окислителем выступает не водород, а азот или сера. Продукты восстановления азотной или серной кислот бывают различными.
Cu + 4HNO3(конц.) → Cu(NO3)2 + 2H2O + 2NO2↑
Fe + 6HNO3(конц.) → t Fe(NO3)3 + 3H2O + 3NO2↑
Ag + 2HNO3(конц.) → AgNO3 + H2O + NO2↑
2P + 5H2SO4 конц → 2H3PO4 + 5SO2 ↑+ 2H2O
2B + 3H2SO4 конц → 2H3BO3 + 3SO2 ↑
S + 2H2SO4 конц → 3SO2 ↑+ 2H2O
Угольная кислота не образуется – получается углекислый газ:
C + 2H2SO4 конц → CO2 ↑ + 2SO2 ↑+ 2H2O
4. Кислоты реагируют с основаниями и основными оксидами.
С нерастворимыми основаниями и соответствующими им оксидами взаимодействуют только растворимые кислоты.
нерастворимое основание + растворимая кислота = соль + вода
Cu(OH)2 + 2HBr → CuBr2 + 2H2O
основный оксид + растворимая кислота = соль + вода
CuO + 2HBr → CuBr2 + H2O
При этом гидроксид меди (II) не взаимодействует с нерастворимой кремниевой кислотой.
Cu(OH)2 + H2SiO3 ≠
С сильными основаниями (щелочами) и соответствующими им оксидами реагируют любые кислотами.
2KOH + H2SiO3 = K2 SiO3 + 2 Н2О
Реакция возможна, только если хотя бы один реагент сильный или кислота растворимая!
То есть нерастворимые основания не реагируют с летучими и или неустойчивыми кислотами
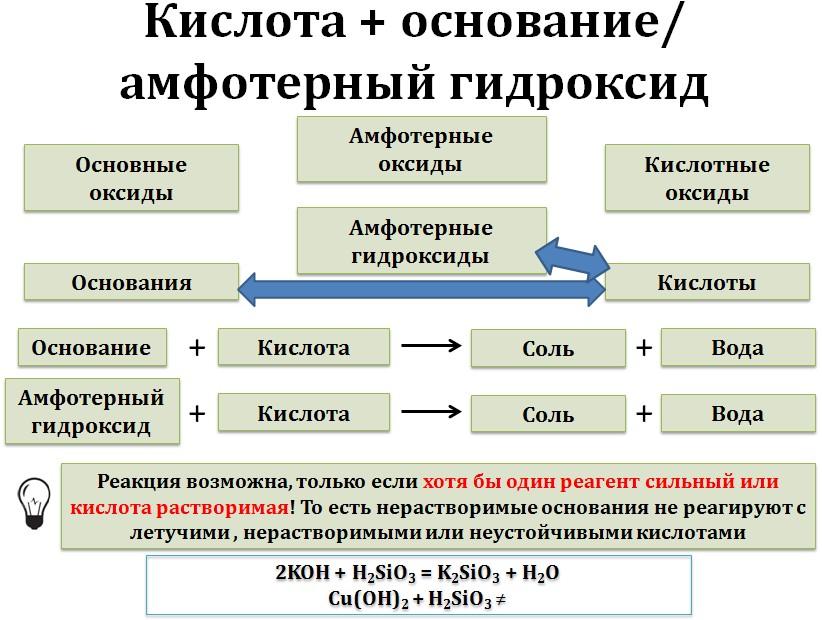
Щёлочи взаимодействуют с любыми кислотами — и сильными, и слабыми. При этом образуются средняя соль и вода. Эти реакции называются реакциями нейтрализации.
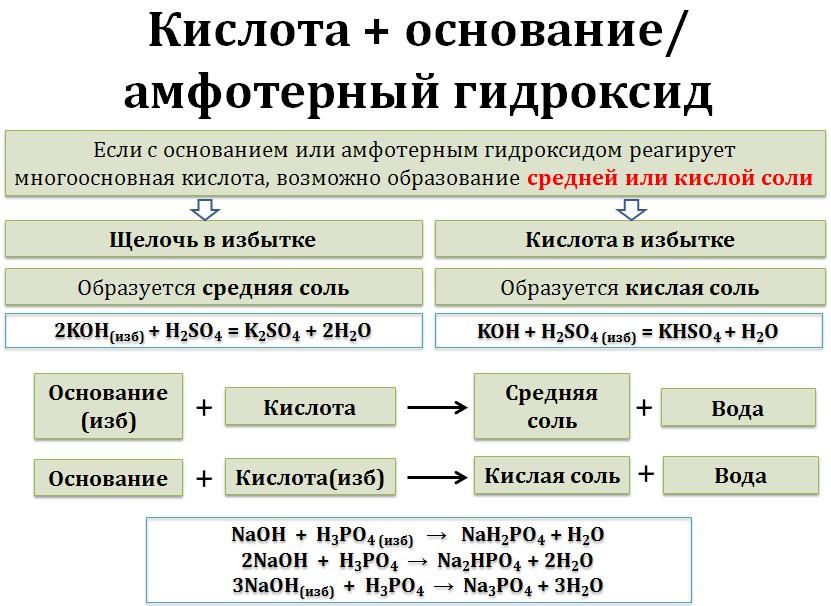
Возможно и образование кислой соли, если кислота многоосновная, при определенном соотношении реагентов, либо в избытке кислоты.
Например, гидроксид натрия при взаимодействии с трёхосновной фосфорной кислотой может образовывать 3 типа солей: фосфаты, дигидрофосфаты, или гидрофосфаты.
В избытке щёлочи образуется средняя соль (фосфат) и вода:
щёлочь(избыток)+ кислота = средняя соль + вода
соотношении количества щелочи и кислоты 3:1 3NaOH + H3PO4 → Na3PO4 + 3H2O
щёлочь + многоосновная кислота(избыток) = кислая соль + вода
(соотношении количеств веществ) реагентов 1:1 образуется дигидрофосфат.
. NaOH + H3PO4 → NaH2PO4 + H2O
соотношении количества щелочи и кислоты 2:1 образуются гидрофосфаты:
2NaOH + H3PO4 → Na2HPO4 + 2H2O
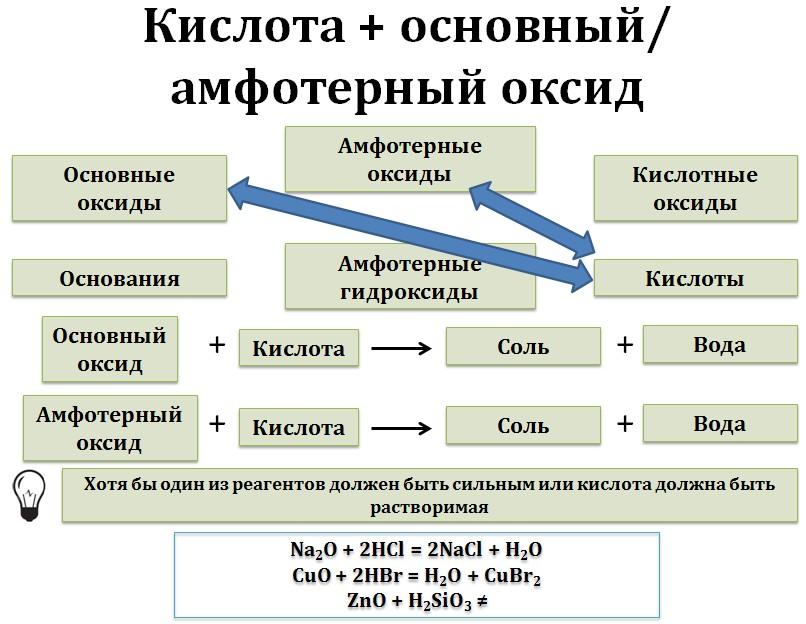
5.Растворимые кислоты взаимодействуют с амфотерными оксидами и гидроксидами.
Растворимая кислота + амфотерный оксид = соль + вода
3H2SO4 + Al2O3 = Al2(SO4)3 +3 H2O
Растворимая кислота + амфотерный гидроксид = соль + вода
Например, уксусная кислота взаимодействует с гидроксидом алюминия:
3CH3COOH + Al(OH)3 → (CH3COO)3Al + 3H2O
6. Некоторые кислоты являются сильными восстановителями. Восстановителями являются кислоты, образованные неметаллами в минимальной или промежуточной степени окисления, которые могут повысить свою степень окисления (йодоводород HI, сернистая кислота H2SO3 и др.).
Например, йодоводород можно окислить хлоридом меди (II), а азотистую кислоту перманганатом калия:
2HI— + 2Cu+2 Cl2 → 2HCl + 2Cu+Cl + I20
2HI— + 2Fe+3 Cl3 → 2HCl + 2Fe2+Cl2 + I20
5HNO2 + 2HMnO4 → 2Mn(NO3)2 + HNO3 + 3H2O
5 HNO2 + 2 KMnO4+ 3 H2SO4 → 2 MnSO4 + K2SO4 + 5 HNO3 + 3 H2O
7. Кислоты взаимодействуют с солями.
Кислоты реагируют с растворимыми солями только при условии, что в продуктах реакции присутствует газ, вода, осадок или другой слабый электролит. Такие реакции протекают по механизму ионного обмена.
Кислота1 + растворимая соль1 = соль2 + кислота2/оксид + вода
Например, соляная кислота взаимодействует с нитратом серебра в растворе:
Ag+NO3— + H+Cl— → Ag+Cl—↓ + H+NO3—
Na2CO3 + 2HCl → 2NaCl + H2O + CO2
Кислоты реагируют и с нерастворимыми солями. При этом более сильные кислоты вытесняют менее сильные кислоты из солей.
Например, карбонат кальция (соль угольной кислоты), реагирует с соляной кислотой (более сильной, чем угольная):
CaCO3 + 2HCl → CaCl2 + H2O + CO2
Кислоты взаимодействуют с кислыми и основными солями. При этом более сильные кислоты вытесняют менее сильные из кислых солей.
кислая соль1 + кислота1 = средняя соль2 + кислота2/оксид + вода
Например, гидрокарбонат калия реагирует с соляной кислотой с образованием хлорида калия, углекислого газа и воды:
KHCO3 + HCl → KCl + CO2 + H2O

5. Кислоты взаимодействуют со своими средними и кислыми и основными солями.
Средние соли реагируют с кислотами с образованием кислых солей
Например: сероводородная кислота реагирует с сульфидом натрия с образованием гидросульфида
H2S + Na2S =2 NaHS
NaCl + HCl ≠
Кислые соли реагируют с кислотами с образованием более кислых солей.
Например: гидрофосфат калия взаимодействует с фосфорной кислотой с образованием дигидрофосфата калия:
H3PO4 + K2HPO4 → 2KH2PO4
При взаимодействии основных солей с кислотами образуются средние соли. Более сильные кислоты также вытесняют менее сильные из солей.
Например, гидроксокарбонат меди (II) растворяется в серной кислоте:
2H2SO4 + (CuOH)2CO3 → 2CuSO4 + 3H2O + CO2
Основные соли могут взаимодействовать с собственными кислотами. При этом вытеснения кислоты из соли не происходит, а просто образуются более средние соли.
Например, гидроксохлорид алюминия взаимодействет с соляной кислотой:
Al(OH)Cl2 + HCl → AlCl3 + H2O
7. Некоторые кислоты разлагаются при нагревании.
Угольная H2CO3, сернистая H2SO3 и азотистая HNO2 кислоты разлагаются самопроизвольно, без нагревания:
H2CO3 ↔ H2O + CO2
H2SO3 ↔ H2O + SO2
2HNO2 ↔ NO + H2O + NO2
Кремниевая H2SiO3, йодоводородная HI кислоты разлагаются при нагревании:
H2SiO3 → H2O + SiO2
2HI ↔ H2 + I2
Азотная кислота HNO3 разлагается при нагревании или на свету:
4HNO3 ↔ O2 + 2H2O + 4NO2






