
Интегрированное занятие «Подгруппа азота» элективного курса «Биогенные элементы нашей жизни»
Автор: Иванова Татьяна Васильевна учитель химии МБОУ СОШ №2
город Батайск
Ростовской области

Скажи мне - и я забуду покажи мне – и я запомню вовлеки меня в процесс - и я пойду отойди – и я буду действовать. Конфуций

г.Батайск МБОУ СОШ №2
Если нет желания учиться
- Существует много приемов воздействия на эмоциональную сферу обучающихся НО! есть три универсальные познавательные эмоции, которые возникают у любого человека, когда он сталкивается с противоречием при овладении новым материалом: удивление, недоумение, восхищение

г.Батайск МБОУ СОШ №2
«Если ученик в школе не научился сам ничего творить, то и в жизни он всегда будет только подражать, копировать, так как мало таких, которые бы, научившись копировать, умели сделать самостоятельное приложение этих сведений»
Л.Н.Толстой
г.Батайск МБОУ СОШ №2
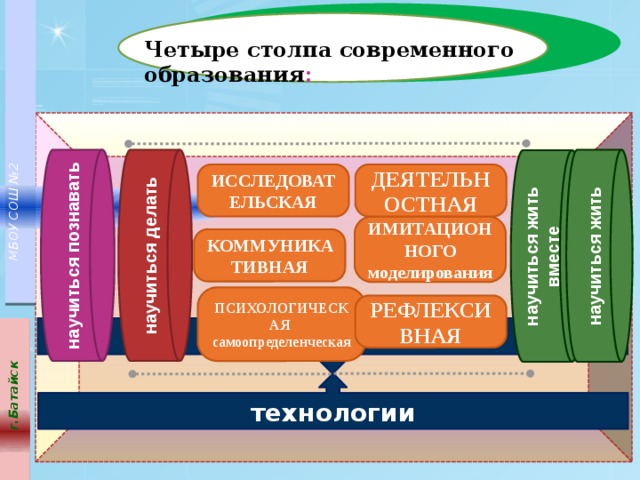
Четыре столпа современного образования :
научиться делать
научиться жить
научиться познавать
научиться жить вместе
ДЕЯТЕЛЬНОСТНАЯ
ИССЛЕДОВАТЕЛЬСКАЯ
ИМИТАЦИОННОГО
моделирования
КОММУНИКАТИВНАЯ
ПСИХОЛОГИЧЕСКАЯ
самоопределенческая
РЕФЛЕКСИВНАЯ
технологии

г.Батайск МБОУ СОШ №2
Принципы обучения
- вне деятельности нет развития;
- знание учениками их собственных возможностей и результатов учения есть обязательные условия их дальнейшего психического развития;
- ученик становится субъектом учебной деятельности лишь на основе таких личностных самообразований, как активность, самостоятельность и общение.
г.Батайск МБОУ СОШ №2
учителя
Задача
Стимулировать интерес
обучающихся к определенным
проблемам, предполагающим владение
определенной суммой знаний
и через деятельность на уроке ,
предусматривающую решение проблем,
показать практическое применение
полученных знаний

Роли участников
образовательного процесса
г.Батайск МБОУ СОШ №2
Ученик – активный
субъект деятельности
Учитель –организатор учебной деятельности, способный к проектированию учебного процесса
Основу ФГОС составляет
методика сотрудничества с
учеником, использование
системно-деятельностного
подхода, практико-
ориентированного метода
обучения

г.Батайск МБОУ СОШ №2
Цели занятия
Надпредметные:
1.Способствовать развитию:
- логического мышления уч-ся,
- умений сравнивать, обобщать данные и делать выводы,
- выбирать критерии для классификации.
2. Создать условия для воспитания взаимопомощи, умения работать в
группе.
3. Способствовать формированию личностных смыслов в усвоении
информации, касающейся бережного отношения к своему здоровью.
Предметные:
Обобщить, закрепить, систематизировать и проверить степень усвоения знаний о свойствах азота, фосфора и их соединений;
умение в составлении ионных уравнений, окислительно-восстановительных реакций;
навыки в решении расчётных и экспериментальных задач.
Цели занятия для ученика:
1. Учиться общаться, работать в группе.
2. Повторить состав, строение, свойства простых веществ, образованных элементами подгруппы азота
3. Проводить химический эксперимент.
4. Знать технику безопасности при работе с веществами.

г.Батайск МБОУ СОШ №2
- групповая работа
Структура занятия
- вводное слово учителя
- выполнение заданий
- рецензии ответов
- оценка групповой работы
- подведение итогов

г.Батайск МБОУ СОШ №2
- Нет “актеров” и “зрителей”
- , все – участники .
Правила совместной работы
СОЦИАЛЬНАЯ
Говорить так, чтобы тебя понимали
Будь активным, стремись к успеху
Критикуются идеи, а не личности
Возражай
Цель деятельности найти лучшее решение

Подгруппа азота
I. Постановка целей
- Вопрос учащимся: «Как сформулировать цель урока?» (учащиеся предлагают свои варианты).
- Цель урока написана на обратной стороне доски.
- На столе учителя набор фигур с цветовыми сигналами (красный, жёлтый, зелёный). Учащиеся выбирают фигуру и садятся в ту группу, где находится соответствующий сигнал.
г.Батайск МБОУ СОШ №2
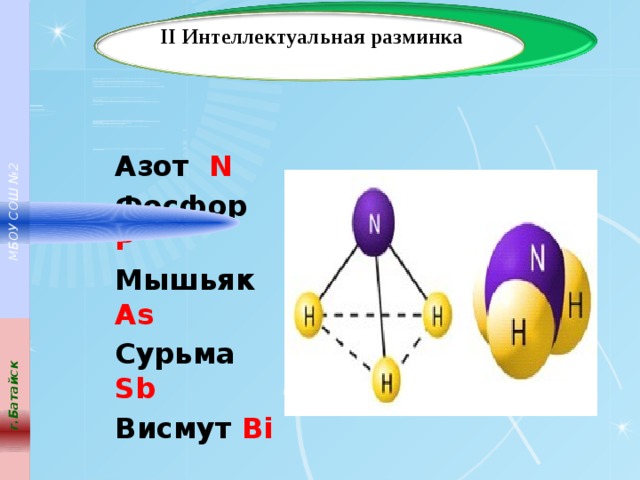
II Интеллектуальная разминка
Азот N
Фосфор P
Мышьяк As
Сурьма Sb
Висмут Bi

г.Батайск МБОУ СОШ №2
Пять знаменитых химиков XVIII в. дали некоему неметаллу, который в виде простого вещества представляет собой газ и состоит из двухатомных молекул, пять разных имен.
- «ядовитый воздух»
- «дефлогистированный
воздух»
- «испорченный воздух»
- «удушливый воздух»
- «безжизненный воздух»
В 1772 году шотландский химик,
ботаник и врач Даниел Резерфорд
В 1772 году английский химик
Джозеф Пристли
В 1773 году шведский химик-
аптекарь Карл Шееле
В 1774 году английский химик
Генри Кавендиш
В 1776 году французский химик
Антуан Лавуазье
И это все об азоте
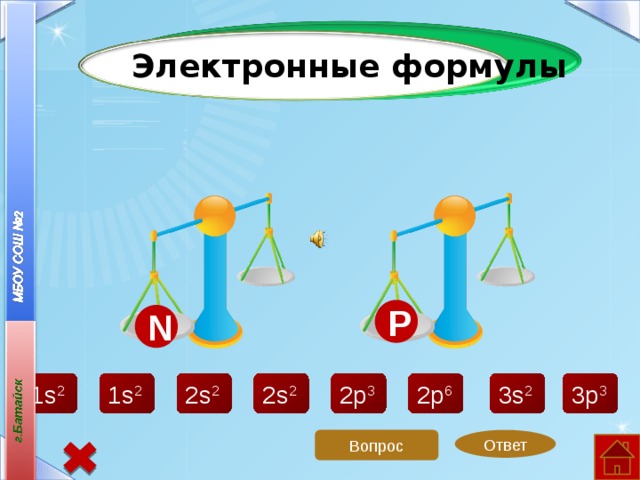
Электронные формулы
P
N
2p 6
3s 2
3p 3
2p 3
2s 2
2s 2
1s 2
1s 2
Вопрос
Ответ
Выбери шар
2
1
3
4
5
Задание
N
P
As
Bi
Sb
83
33
15
7
14,007
121,75
74,922
30,974
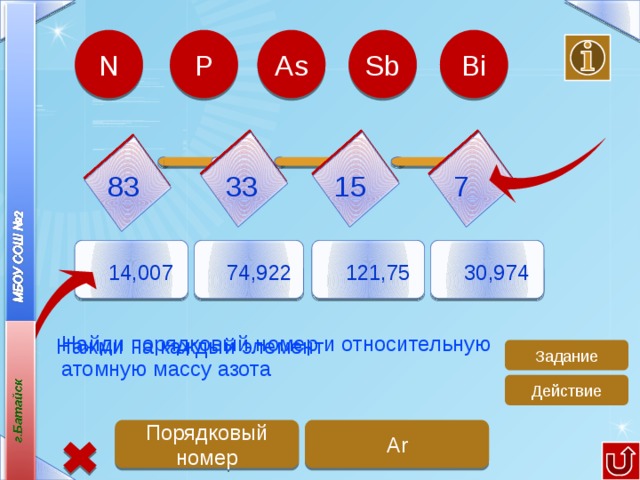
Найди порядковый номер и относительную атомную массу азота
Нажми на каждый элемент
Задание
Действие
Порядковый номер
Ar
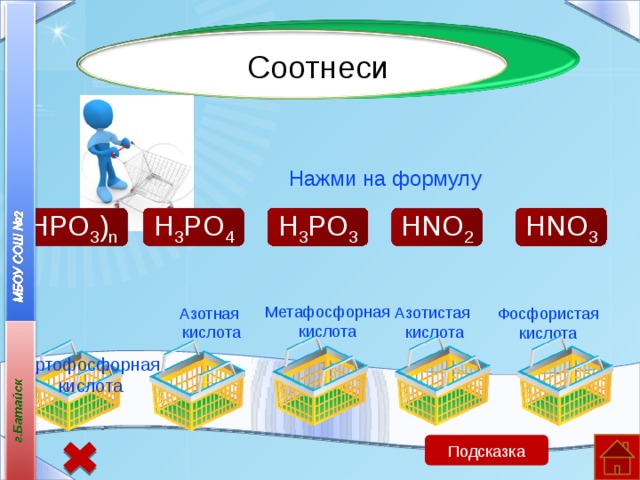
Соотнеси
Нажми на формулу
H 3 PO 3
HNO 3
(HPO 3 ) n
H 3 PO 4
HNO 2
Ортофосфорная кислота
Метафосфорная кислота
Азотистая
кислота
Азотная
кислота
Фосфористая кислота
Подсказка

Таинственный элемент
Этот элемент открыт совершенно случайно
8
В 1669 году алхимиком Брандом
1
5
7
6
4
3
2
с
о
о
е
с
в
н
т
Назван « phosphorus» - фосфор
Зашифрованное слово – это перевод слова фосфор с греческого
Нужная информация
Иллюстрация
Часто встречается в русской химической литературе XIX века
ответ

Таинственный элемент
1
С
С
Слово укоренилось только в русском и французском языках
е
2
е
3
л
Словесный гибрид
4
и
5
т
Образовано от латинского – селитра и греческого - рождение
р
6
р
7
о
Пытались перевести это слово на русский язык
8
т
Нужная информация
9
в
в
10
о
о
Иллюстрация
Это слово было неудобопроизносимым
11
р
р
ответ

Таинственный элемент
Азот открыт почти одновременно несколькими исследователями
3
1
2
9
8
7
6
5
4
Название от греческой отрицательной приставки «а» и слова «зоэ»
и
о
т
н
л
в
о
Г
р
т
л
в
Название означало «безжизненный»
Название часто встречалось в русской химической литературе начала XIX века
Нужная информация
Иллюстрация
ответ
г.Батайск МБОУ СОШ №2
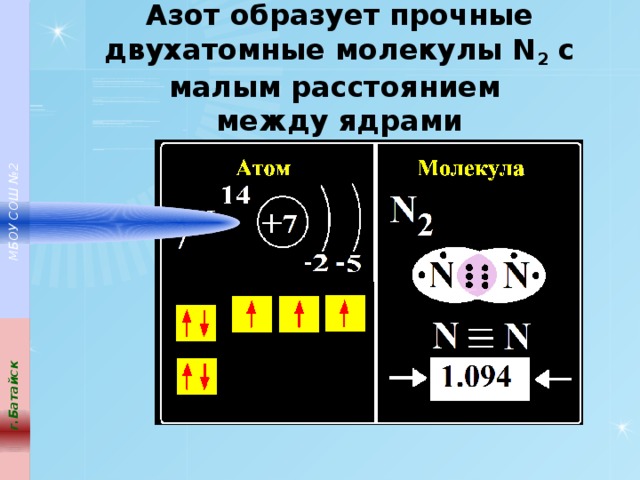
Азот образует прочные двухатомные молекулы N 2 с малым расстоянием между ядрами
г.Батайск МБОУ СОШ №2
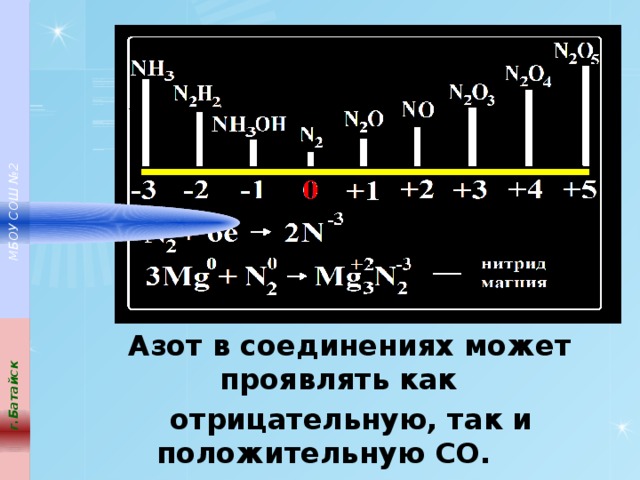
Азот в соединениях может проявлять как
отрицательную, так и положительную СО.

г.Батайск МБОУ СОШ №2
Почему Даниэль Резерфорд назвал открытый им газ «зловредным», а Антуан Лавуазье дал ему общее название - азот, т.е. «безжизненный»?
Чем обусловлена химическая инертность азота?
В какое соединение превращается азот в верхних слоях атмосферы во время грозовых разрядов?

г.Батайск МБОУ СОШ №2
Как получают азот в промышленности?
Почему азот называют «элементом жизни»?
Что такое «нашатырный спирт»? Для чего его используют?
Какие свойства аммиака лежат в основе его применения в холодильных установках?

- 1. Степень окисления азота в оксиде NO 2 равна.
- А) +2; К Б) +4; А В) -4. Н
- 2. Как называются соли азотной кислоты
- А) нитраты; М Б) нитриты; И В) нитриды. Л
- 3. В каких из указанных реакций азот N 2 играет роль восстановителя?
- А) N 2 + 3Mg = Mg 3 N 2 ; К Б) N 2 + 3F 2 = 2NF 3 ; М В) N 2 + 3H 2 = 2NH 3 Н
III. Прохождение маршрута командами
- По результатам выполненных заданий должно получиться слово. Ответы закодированы буквами русского алфавита.
- I команда
25

- III. Прохождение маршрута командами
- 4. С каким из указанных веществ взаимодействует конц. HNO 3 с образованием NO 2 ?
- А) Сu; И Б) ZnO; А В) Ag. О
- 5. Сумма коэффициентов в уравнении реакции NH 3 + O 2 = N 2 +H 2 O равна:
- А) 7; Т Б) 10; С В) 15. А
- 6. Сколько молей азотной кислоты расходуется на с 10 г карбоната кальция?
- А) 0,1 моль; М Б) 2 моль; У В) 0,2 моль. К (АММИАК)

II команда
- Степень окисления азота в оксиде азота N 2 O равна
- А) +2; К Б) +1; Н В) +4. О
- 2. Как называются соли азотистой кислоты
- А) нитраты; А Б) нитриты; И В) нитриды. В
- 3. В каких из указанных реакций азот N 2 играет роль окислителя?
- А) N 2 + 3Mg = Mg 3 N 2 ; Т Б) N 2 + 3F 2 = 2NF 3 ; Б В) N 2 + O 2 = 2NO В

II команда
- 4. В молекуле азота связь
- А) одинарная; Л Б) двойная; С В) тройная. Р
- 5. Сумма коэффициентов в уравнении реакции NH 3 + O 2 = NO + H 2 O равна
- А) 19; А Б) 9; У В) 12. И
- 6. Какой объём углекислого газа выделяется в реакции азотной кислоты с 21,2 г карбоната натрия?
- А) 2,24 л; М Б) 44,8 л; Х В) 4,48 л Т (НИТРАТ)

III команда
- 1. Степень окисления фосфора в оксиде Р 2 О 5 равна
- А) +3; А Б) +5; Ф В) – 3. К
- 2. Как называются соли фосфорной кислоты?
- А) фосфиды; А Б) фосфориты; У В) фосфаты. О
- 3. В каких из указанных реакций фосфор играет роль восстановителя?
- А) 2Р+8Н 2 О=2Н 3 РО 4 +5Н 2 С Б) 3Са+2Р=Са 3 Р 2 М В)3Nа+Р= Nа 3 Р Н
III команда
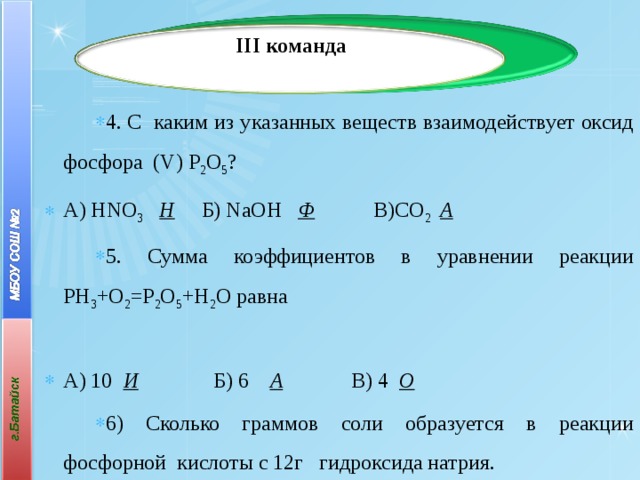
- 4. С каким из указанных веществ взаимодействует оксид фосфора (V) Р 2 О 5 ?
- А) НNО 3 Н Б) NаОН Ф В)СО 2 А
- 5. Сумма коэффициентов в уравнении реакции РН 3 +О 2 =Р 2 О 5 +Н 2 О равна
- А) 10 И Б) 6 А В) 4 О
- 6) Сколько граммов соли образуется в реакции фосфорной кислоты с 12г гидроксида натрия.
- А) 16,4г Д Б)98г К В) 19,6г Т (ФОСФИД)

IV. Защита полученных результатов
Представители команд защищают выполненные задания. Учитель подводит итог работы команд.
NH 3
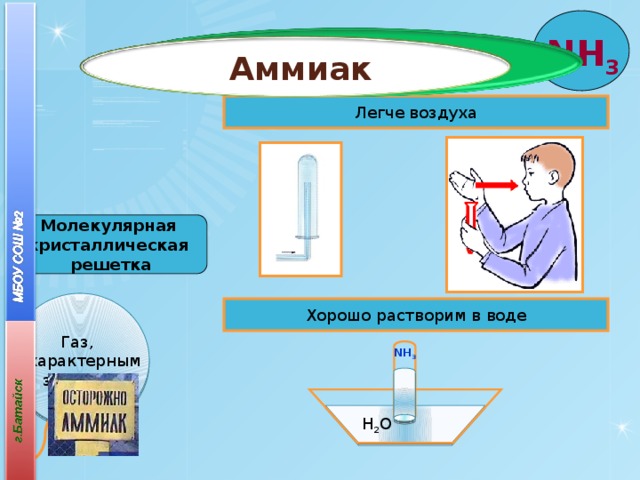
Аммиак
Легче воздуха
Молекулярная
кристаллическая
решетка
Газ,
с характерным
запахом.
Хорошо растворим в воде
NH 3
H 2 O
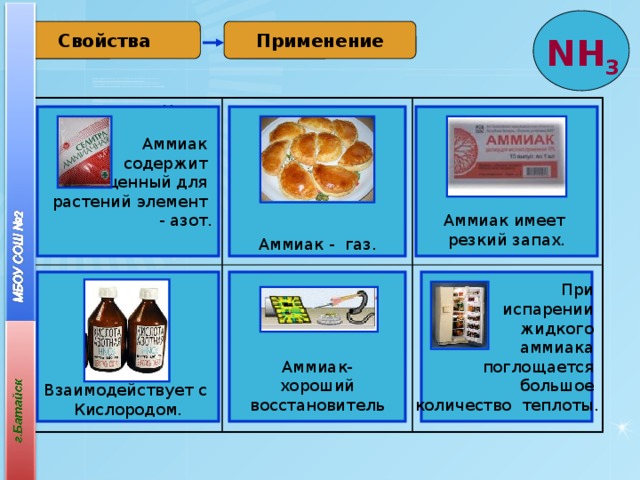
Свойства
Применение
NH 3
Рассчитайте массовую долю азота в аммиачной селитре
Запишите уравнение реакции разложения гидрокарбоната аммония
Как осуществить превращения?
NH 3 → NO → NO 2 HNO 3
Составьте окислительно-восстановительную реакцию взаимодействия хлорида аммония с оксидом меди.
Рассчитайте объем аммиака для приготовления 50г 5% - ного нашатырного спирта (при н.у.)
Какой объем при нормальных условиях будет занимать 1 кг жидкого аммиака.
Аммиак
Аммиак - газ.
содержит
ценный для
растений элемент
- азот.
Аммиак имеет
резкий запах.
Взаимодействует с
При
испарении
Кислородом.
жидкого
аммиака
поглощается
Аммиак-
хороший
большое
восстановитель
количество теплоты.
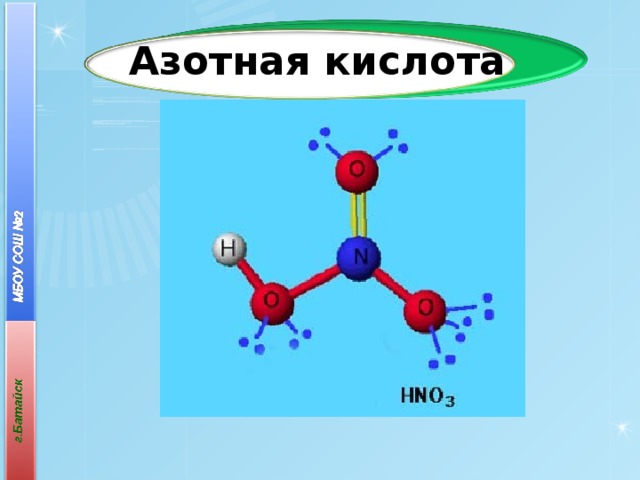
Азотная кислота

Строение
Одна связь с кислородом образуется по донорно-акцепторному механизму, но из-за близости расположения атомов в молекуле становятся равноценными.

Применение
Азотная кислота широко используется для производства азотных удобрений, искусственных волокон, органических красителей, лаков и взрывчатых веществ.
Фосфор
- Р Фосфор
- ( Phosphorus-Cветоносец)
- неметалл,
- Ar=31
- V группа, главная подгруппа
- 3 период, 3 ряд
- степени окисления -3.0,+1,+3,+5.
- оксиды Р 2 О 3 и Р 2 О 5 - оба оксида кислотные
- Кислоты:
- H 3 PO 3 –фосфористая кислота H 3 PO 4 –фосфорная кислота
- летучее водородное соединение РН 3 -газ фосфин ( связь ковалентная почти неполярная)

- Красный фосфор применяют для изготовления спичек и как наполнитель (пары) в лампах накаливания для производства удобрений и кормовых добавок для животных.

V .Рефлексия
- Учащиеся высказывают мнение об уроке. Учитель подводит итог урока, выставляет оценки.

БЛАГОДАРЮ ЗА ВНИМАНИЕ !!!





