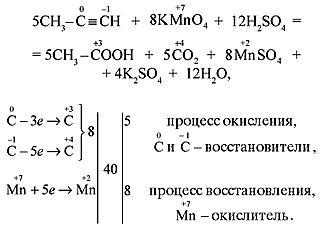
Окисление алкенов
При мягком окислении алкены , в нейтральной или слабощелочной средах окисление сопровождается образованием диолов. (Разрывается только Пи связь)
2KMnO4 + 3 H2C=CH2 + 4H2O == 3 CH2-OH-CH2-OH + 2 MnO2 + 2 KOH
При более жёстком(концентрированным раствором перманганата калия KMnO4 в кислой среде,) в карбоновые кислоты, кетоны. Разрывается углеродная цепь по двойной связи и образуются две кислоты. (В сильно щелочной среде, две соли). Или, если двойная связь при первом углероде, кислота и углекислый газ. (В сильно щелочной среде а)Если молекула алкена симметрична и двойная связь содержится в середине молекулы, то при окислении образуется только одна кислота:
5CH3CH=CHCH2CH3 + 8KMnO4 + 12H2SO4 ![]() 5CH3COOH + 5C2H5COOH + 8MnSO4 + 4K2SO4 + 17H2O
5CH3COOH + 5C2H5COOH + 8MnSO4 + 4K2SO4 + 17H2O
б) Если двойная связь находится на конце молекулы (например, у бутена-1), то одним из продуктов окисления является муравьиная кислота, легко окисляющаяся до углекислого газа и воды
|
|
|
в)Если при двойной связи 2 радикала-образуются кетоны 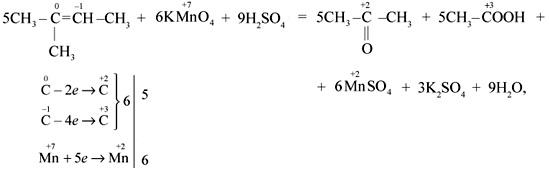
г) Особенностью окисления алкенов, в которых атомы углерода при двойной связи содержат по два углеродных радикала, является образование двух кетонов:
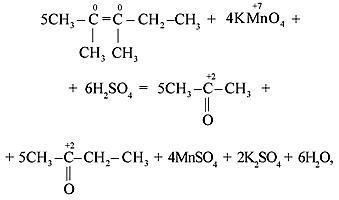
Окисление алкинов
Алкины окисляются в более жёстких условиях, чем алкены, поэтому они окисляются с разрывом тройной связи. В результате реакции образуются кислоты и углекислый газ
|
|
|
Ацетилен может быть окислен перманганатом в нейтральной среде до аксалата
3CH≡CH +8KMnO4 → 3KOOC-COOK оксалат калия +8MnO2↓+ 2KOH+ 2H2O
Его гомологи-

В кислой среде, окисление идёт до щавелевой кислоты или до углекилого газа
5H-C≡C-H + 8KMnO4 + 12H2SO4→5 HOOC-COOH +2 MnSO4 + 4H2O + K2SO4(щавелевая кислота)
H-C≡C-H + 2KMnO4 +3H2SO4→2CO2 +2 MnSO4 + 4H2O + K2SO4
Бензол и его гомологи
При окисления аренов в кислой среде следует ожидать образования кислот, а в щелочной – солей. Гомологи бензола с одной боковой цепью (независимо от ее длины) окисляются сильным окислителем до бензойной кислоты по α -углеродному атому. Гомологи бензола при нагревании окисляются перманганатом калия в нейтральной среде с образованием калиевых солей ароматических кислот.
5C6H5–CH3 + 6KMnO4 + 9H2SO4 = 5C6H5COOH + 6MnSO4 + 3K2SO4 + 14H2O,
5C6H5–C2H5 + 12KMnO4 + 18H2SO4 = 5C6H5COOH + 5CO2 + 12MnSO4 + 6K2SO4 + 28H2O, C6H5–CH3 + 2KMnO4 = C6H5COOK + 2MnO2 + KOH + H2O.
C6H5CH2CH3 + 4KMnO4 = C6H5COOK + K2CO3 + 2H2O + 4MnO2 + KOH
Если в молекуле арена несколько боковых цепей, то в кислой среде каждая из них окисляется по a-углеродному атому до карбоксильной группы, в результате чего образуются многоосновные ароматические кислоты:
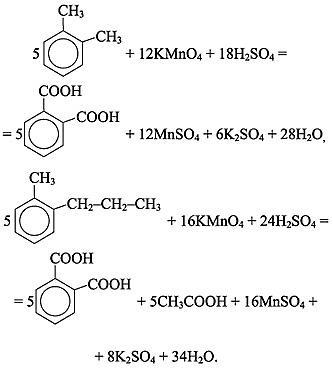
4) Окисление кумола: а)кислородом в присутствии катализатора (кумольный способ получения фенола):
C6H5CH(CH3)2 +O2 + H2SO4→ C6H5-OH фенол + CH3-CO-CH3 ацетон
б)перманганатом вкислой среде окисляется до бензойной кислоты
5C6H5CH(CH3)2 + 18KMnO4 + 27H2SO4 → 5C6H5COOH + 42H2O + 18MnSO4 + 10CO2 + K2SO4
Следует обратить внимание на то, что при мягком окислении стирола перманганатом калия КMnO4 в нейтральной или слабощелочной среде происходит разрыв π -связи ,образуется гликоль (двухатомный спирт).
3C6H5−CH═CH2+2 KMnO4+4 H2O→3C6H5−CН(OH)- CН2(OH) → 2 MnO2+2КОН
В результате реакции окрашенный раствор перманганата калия быстро обесцвечивается и выпадает коричневый осадок оксида марганца (IV). Окисление же сильным окислителем – перманганатом калия в кислой среде – приводит к полному разрыву двойной связи и образованию углекислого газа и бензойной кислоты, раствор при этом обесцвечивается. C6H5−CH═CH2+2 KMnO4+3 H2SO4→C6H5−COOH + CO2 ↑ + K2SO4 + 2 MnSO4 +4 H2O
Спирты
Следует помнить, что: 1) первичные спирты окисляются до альдегидов:
3CH3–CH2OH + K2Cr2O7 + 4H2SO4 = 3CH3–CHO + K2SO4 + Cr2(SO4)3 + 7H2O;
2) вторичные спирты окисляются до кетонов:
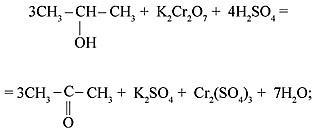
3) для третичных спиртов реакция окисления не характерна.
При окислении метанола подкисленным раствором перманганата калия или дихромата калия образуется CO2.
Первичные спирты при окислении в зависимости от условий протекания реакции могут образовать не только альдегиды, но и кислоты.
Например, окисление этанола дихроматом калия на холоду заканчивается oбразованием уксусной кислоты, а при нагревании – ацетальдегида:
3CH3–CH2OH + 2K2Cr2O7 + 8H2SO4 = 3CH3–COOH + 2K2SO4 + 2Cr2(SO4)3 + 11H2O,
3CH3–CH2OH + K2Cr2O7 + 4H2SO4 3CH3–CHO + K2SO4 + Cr2(SO4)3 + 7H2O
Помним о влиянии среды на продукты реакций окисления спиртов, а именно: горячий нейтральный раствор KMnO4 (или избыток окислителя в той же среде)окисляет метанол до карбоната калия, а остальные спирты – до солей соответствующих карбоновых кислот:

Окисление гликолей
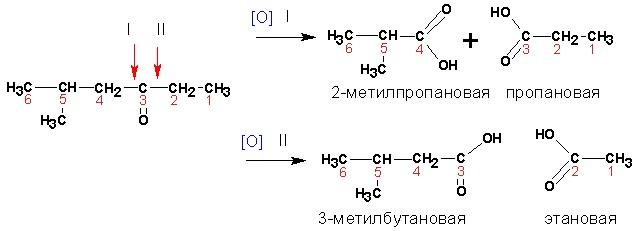
1,2-Гликоли легко расщепляются в мягких условиях при действии иодной кислоты. В зависимости от строения исходного гликоля продуктами окисления могут быть альдегиды или кетоны:
![]()
Если три или более ОН-групп связаны с соседними атомами углерода, то при окислении иодной кислотой средний или средние атомы превращаются в муравьиную кислоту Окисление гликолей перманганатом калия в кислой среде проходит аналогично окислительному расщеплению алкенов и также приводит к образованию кислот или кетонов в зависимости от строения исходного гликоля.
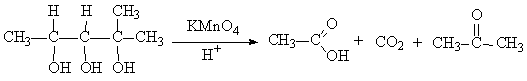
Альдегиды и кетоны
легче, чем спирты, окисляются в соответствующие карбоновые кислоты не только под действием сильных окислителей (кислород воздуха, подкисленные растворы KMnO4 и K2Cr2O7), но и под действием слабых (аммиачный раствор оксида серебра или гидроксида меди(II)): 5CH3–CHO + 2KMnO4 + 3H2SO4 = 5CH3–COOH + 2MnSO4 + K2SO4 + 3H2O,
3CH3–CHO + K2Cr2O7 + 4H2SO4 = 3CH3–COOH + Cr2(SO4)3 + K2SO4 + 4H2O,
CH3–CHO + 2[Ag(NH3)2]OH CH3–COONH4 + 2Ag + 3NH3 + H2O
Особое внимание!!! Окисление метаналя аммиачным раствором оксида серебра приводит к образованию карбоната аммония, а не муравьиной кислоты:
HCHО + 4[Ag(NH3)2]OH = (NH4)2CO3 + 4Ag + 6NH3 + 2H2O.

 5CH3COOH + 5C2H5COOH + 8MnSO4 + 4K2SO4 + 17H2O
5CH3COOH + 5C2H5COOH + 8MnSO4 + 4K2SO4 + 17H2O