Государственное учреждение
«Луганская школа I – III ступеней № 18»
Раздаточный материал
к бинарному уроку
химии и математики
2016
Табличное оформление задачи №5
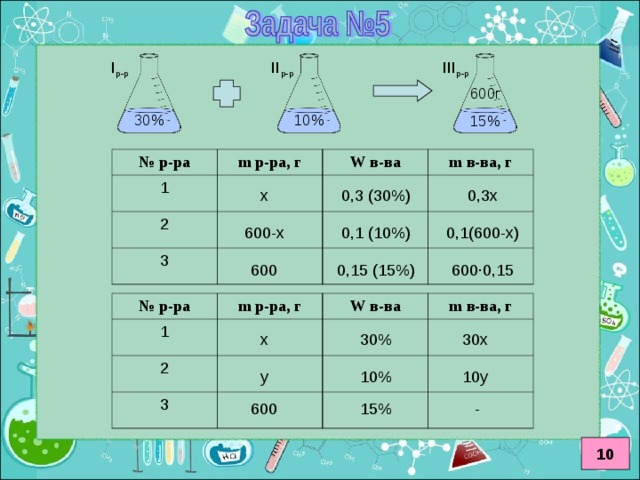
I способ
| № р-ра | m р-ра, г | W в-ва | m в-ва, г |
| 1 | | | |
| 2 | | | |
| 3 | | | |
II способ
| № р-ра | m р-ра, г | W в-ва | m в-ва, г |
| 1 | | | |
| 2 | | | |
| 3 | | | |
------------------------------------------------------------------------------------------------------------------------
Основные формулы
| |
| |
| |
| |
Алгоритм решения задач
Внимательно прочитать текст задачи, стараясь понять ее суть.
Выполнить химическую часть задачи:
составить уравнение реакции;
записать условие задачи, используя общепринятые обозначения физико-химических величин;
провести запись вспомогательных величин, согласно условию задачи;
исследовать текст задачи;
наметить план решения задачи.
Выполнить математическую часть задачи:
подобрать наиболее рациональный способ решения;
провести необходимые расчеты;
осуществить проверку полученного результата (правильность хода выполненного решения);
записать ответ.
------------------------------------------------------------------------------------------------------------------------
Задачи
Соблюдая правила ТБ проведите реакцию нейтрализации между соляной кислотой и гидроксидом натрия и рассчитайте массу образовавшейся соли, если масса кислоты составляет 7,3г.
Соблюдая ТБ, проведите качественную реакцию на соляную кислоту и определите ее массу, если известно, что в результате нейтрализации получили 1,505·1023 молекул осадка.
Проведите реакцию между алюминием и соляной кислотой и определите, какое количество алюминия прореагирует с избытком соляной кислоты для получения 5,6л водорода (н.у.). Рассчитайте число молекул кислоты израсходованной в данной реакции.
Термохимическое уравнение реакции оксида меди (II) с соляной кислотой:
![]()
Сколько теплоты выделится при растворении 200г оксида меди (II) в соляной кислоте. Проделайте данную реакцию, соблюдая правила ТБ.
Смешали 30% раствор хлорида натрия с 10% его раствором и получили 600г 15% раствора. Сколько граммов каждого раствора было взято?
Для получения раствора хлорида калия необходимое количество карбоната калия растворили в 8% растворе соляной кислоты. Рассчитайте массовую долю соли в полученном растворе.
К 150г 20% раствора соляной кислоты прилили 200мл воды. Каково процентное содержание кислоты во вновь полученном растворе?
Смешали 140г раствора соляной кислоты с 200г 3% раствора этой же кислоты. Каково процентное содержание соляной кислоты во вновь полученном растворе?
Определите сколько граммов 20% и 50% раствора хлорида калия надо взять, чтобы получить 150г 30% раствора соли.
В избытке соляной кислоты растворили магний массой 6г и цинк массой 6,5г. Какой объем водорода, измеренный при нормальных условиях, выделится при этом?
Какая масса хлорида алюминия образуется при взаимодействии хлороводорода массой 7,3г с аммиаком массой 5,1г? Какой газ останется в избытке? Определите массу избытка?
Какой объем займет при нормальных условиях газовая смесь, содержащая водород массой 1,4г и азот массой 5,6г?
Сайт школы: http://school18lg.wixsite.com/school18lg
Химические свойства соляной кислоты

Химические свойства соляной кислоты